化学基礎の基本練習 P Page 12 1714 19 イオン反応式 学習日 月 日 まとめ ① イオン反応式 イオンが関係する反応を式で表すとき,反応しないイオンを示さず,反応したイ オンだけを㋐ で示した化学反応式。・イオン結合でできている物質は「組成式」によって表現(結晶ができてしまい、分子と違って切れ目がないため) ・構成している元素の種類と、数の比によって表現 ・正負の電荷を打ち消すようにできている このレッスンの動画一覧 1.組成式 化学基礎で最初の方に習う基礎的な内容の「組成式」と「分子式」ですが、意外とその違いが見分けづらいです。 例えば、CO2は分子式でSiO2は組成式です。 もちろん、わかる人には当たり前なんですが、わからない人にとってはなかなか厳しい内容です。 また、組成式は金属結晶やイオン結晶を表すためのものだと思っています。 そのような間違った認識をして
結晶構造とは コトバンク
組成式 イオン 結晶 一覧
組成式 イオン 結晶 一覧-<その他の組成式> 炭酸水素ナトリウム NaHCO 3 硫酸水素ナトリウム NaHSO 4 亜硫酸水素ナトリウム NaHSO 3 酢酸ナトリウム CH 3 COONa 二酸化ケイ素 SiO 2 イオン結合による結晶です。多数の陽イオンと陰イオンが規則正しく配列して固体に なっています。化学式は組成式で表します。 イオン結晶の見分け方 金属元素と非金属元素 が含まれた物質はイオン結晶です。例えば、NaCl,BaSO 4 など。 例外として、 アンモニウムイオン NH 4 を



イオン結合でできるイオン結晶を表す組成式って何
組成 式 一覧。 水素カリウム• ) 組成式〜構造式まで化学式まとめ 化学式には、大きく分けて ・分子式 ・組成式(実験式) ・構造式 ・示性式 があり、特に注意するところは『共有結合結晶が組成式で表される』、『構造式には何通りもの描き方がこの記事では、 化学式の作り方、化学式の書き方のルール、化学式の名前の付け方や覚え方、中学生の子が覚えて 高1化学組成式の問題です!次のイオンからできる物質の組成式を書け。 1 ba2+ と co3(2-)2 ca2+ と oh3 nh4+ と cl4 nh4+ と co3(2-)5イオン 結晶 組成 式 井村 シンクロ クラブ 高校化学 結合 イオン結合 組成式の書き方 オンライン無料塾 ターンナップ Youtube 高校化学基礎 組成式の書き方 映像授業のtry It トライイット
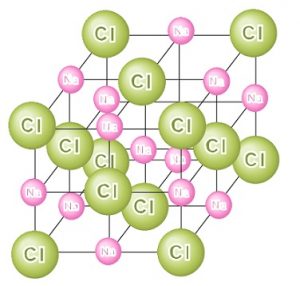
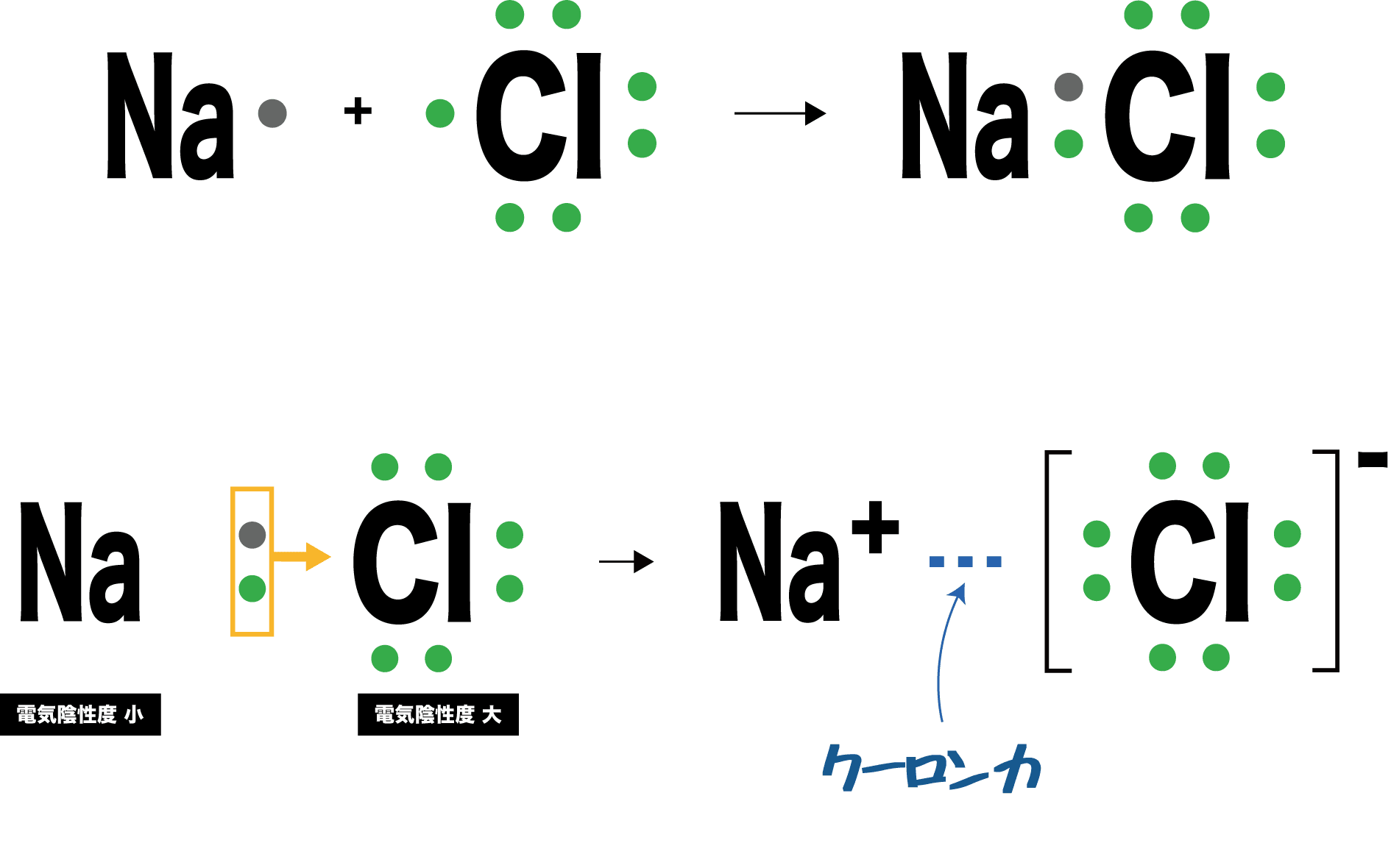
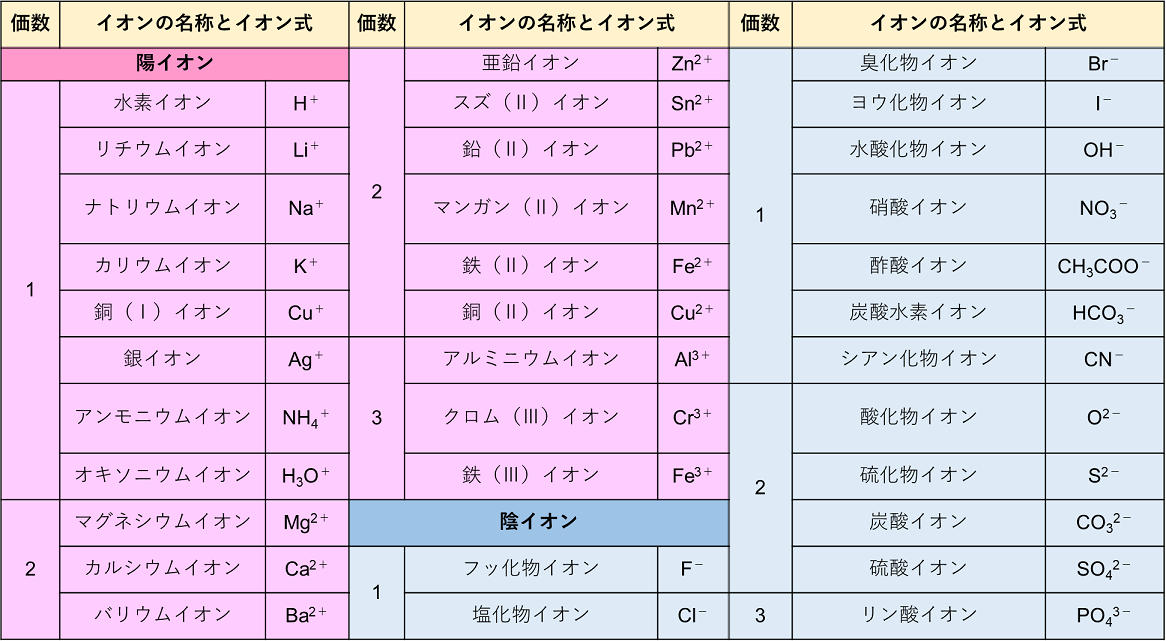
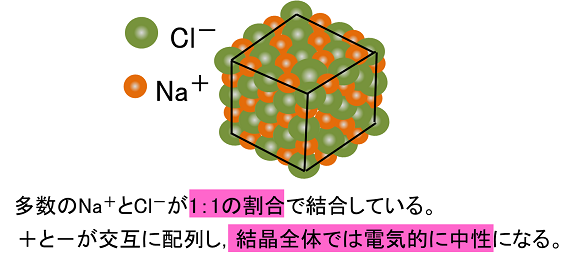
イオン式 名称 貴ガス 2 イオン結合とイオン結晶 A イオン結合 (化p8/化基p56) ・陽イオンと陰イオンの結合 = ① ( ② によって引き合っている) 組成式とは? これは、NaClのイオン結晶である岩塩です。 これは、NaとClがずっとイオン結合を連ねて、このような目に見える形になっているのです。 このように、無限にイオン結合が続いているわけですよ。 じゃあ、 分子式 みたいにその塊の原子の数を全部書き出したとします。 すると、この岩塩には、Na とCl – が日本の人口以上に詰まっているわけですよ2.イオン結晶 原子、分子、イオンなどの粒子が規則正しく並んでできた固体を結晶といい、イオン結合でできた結晶をイオン結晶という。 イオン結晶には次のような共通の性質がある 陽イオンと陰イオンの静電気的な引力が強いため、融点が高い
高校化学 イオン結合とイオン結晶と組成式の作り方 / 化学 by イオン式 クエン酸の化学式・構造式や性質を詳しく解説🍋 クエン酸は酸味を持つ物質で、レモンなどの柑橘類に多く含まれるほか、食品添加物としても多用されます。 安全性が高く、水垢などを落とす洗剤としても普及しました。 この記事では、 クエン酸のイオン式とは?イオン式の一覧と読み方を一挙公開! 化学 組成式とは?入試で必要な知識と勘違いするポイントをまとめ 組成式・・・・ 普通は、NaClのように+イオン 教えて!goo;



Q Tbn And9gcssqz9tuetvs62uxrdhpvyjzko2wugy0iaegnq0qyi2 Avo8wmm Usqp Cau



イオン結晶 共有結合の結晶 分子結晶まとめ 理系ラボ
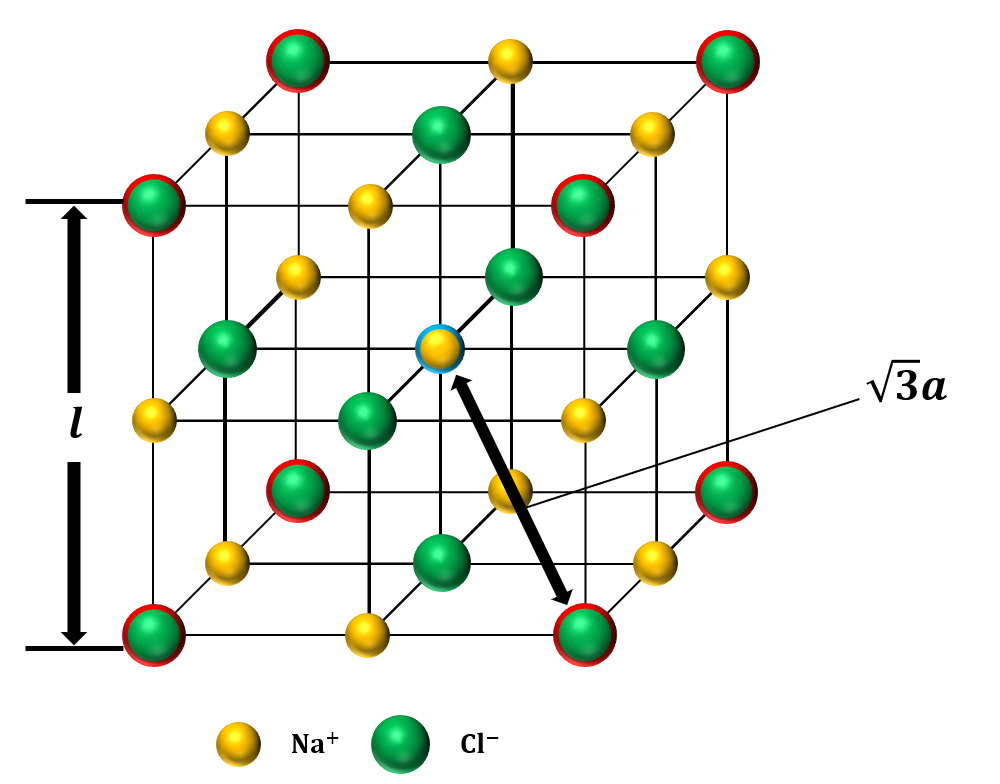
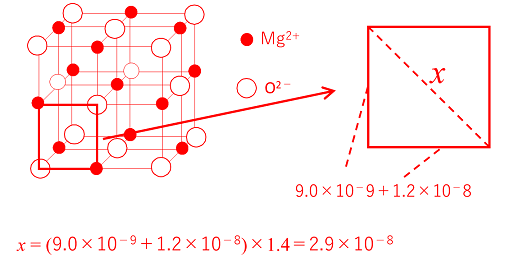
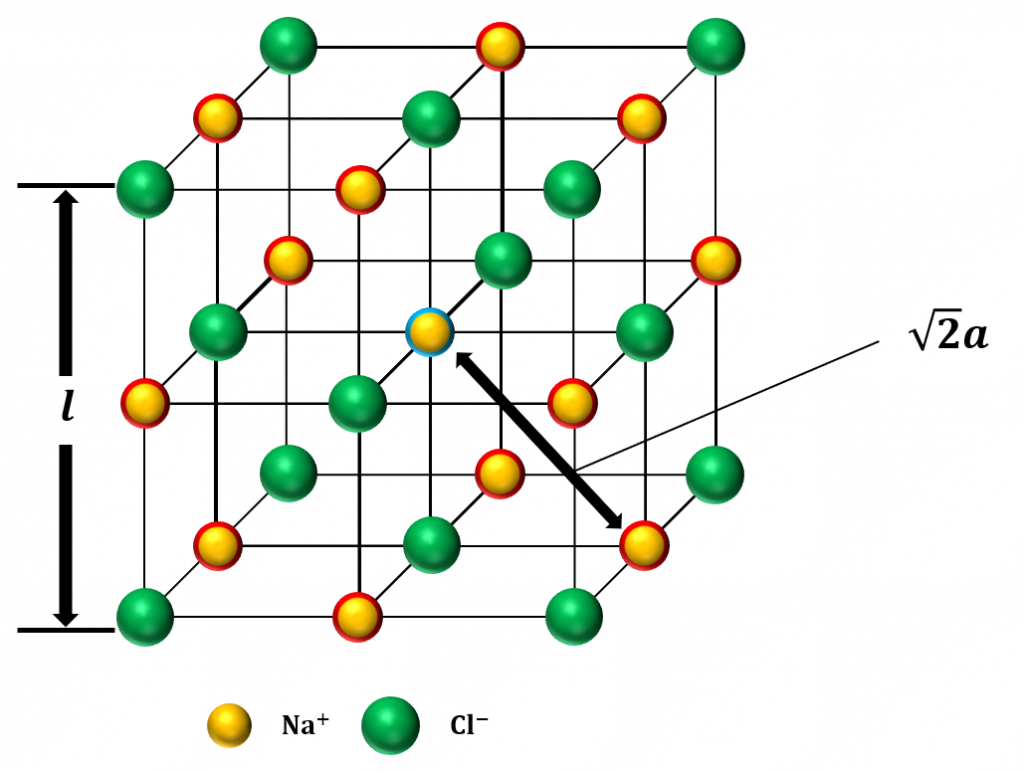
&o 1 2 2 & &o &o 1 1 2 & 2 2 分子と共有結合 共有結合 非金属元素どうしの結合。 原子間で不足分の電子を出し合って共有することによってできる結合。1つの分子を構成する元素とその数をただ単に羅列したものであらわされます。 酢酸:C₂H₄O₂やグルコース:C₆H₁₂O₆など。 最も、酢酸やグルコース他は組成式でも分子式でも構造式でもなんだってあらわされます。 ここで勘違いしてほしくないのは イオン式や組成式、分子式は単なる表し方にすぎない ということ。 この分野で苦手意識を持っている学生は結晶の構造は,陽イオンや陰イオンの大きさ,イオンの価数などで決まります。 組成式 塩化ナトリウムの結晶の中には,ナトリウムイオンNa+と塩化物イオンCl-が同じ数だけ含まれています。 例えば,1 gの塩化ナトリウムNaClの結晶があると,その中には約1022個のNa+とCl-がそれぞれ含まれています。 しかし,NaClとは書き




炭酸ナトリウム Na2co3 の化学式 分子式 構造式 電子式 イオン式 分子量は 炭酸ナトリウムの工業的製法




なぜaの単位格子の角1つは4分の1なのにbの単位格子の角1つは8分の1なのですか Clear
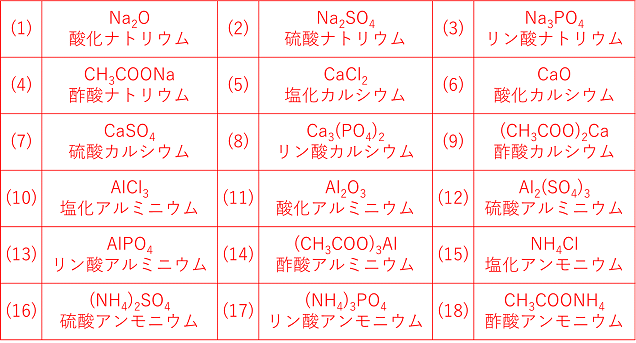
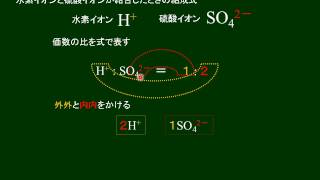
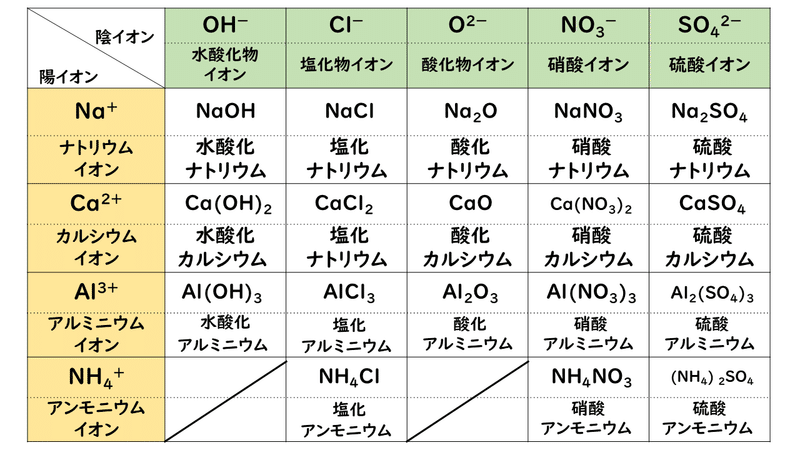
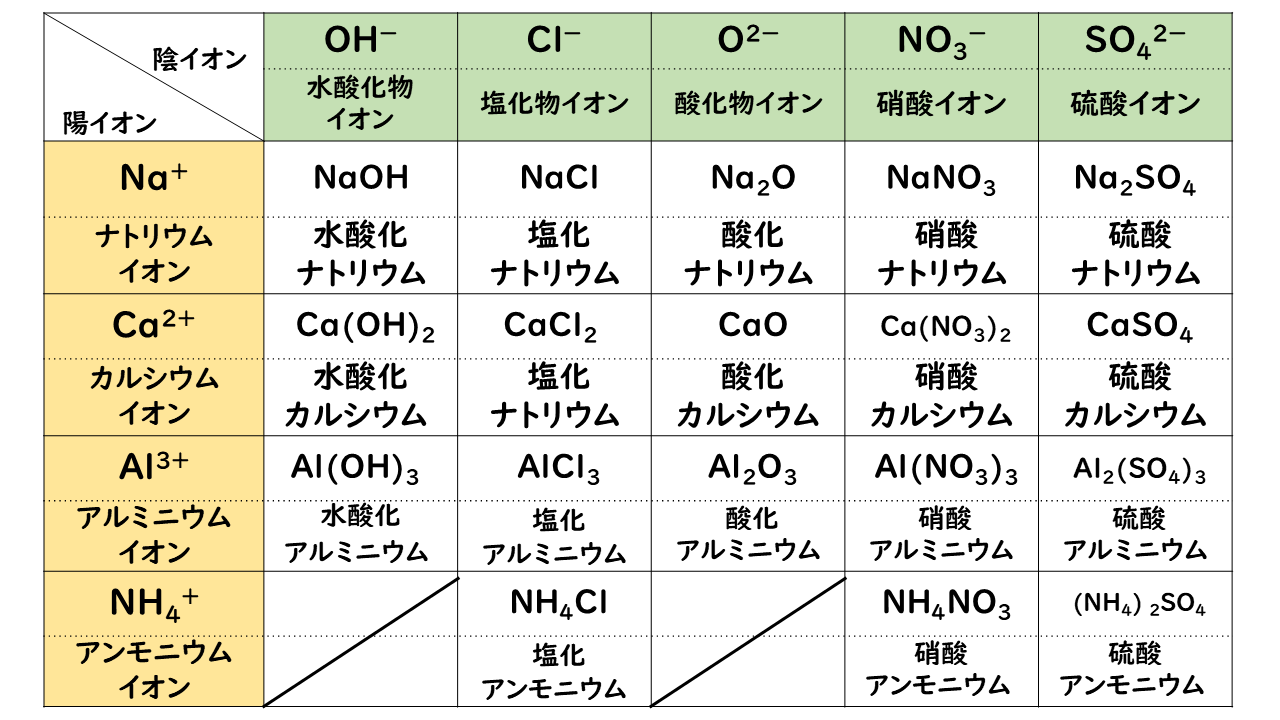
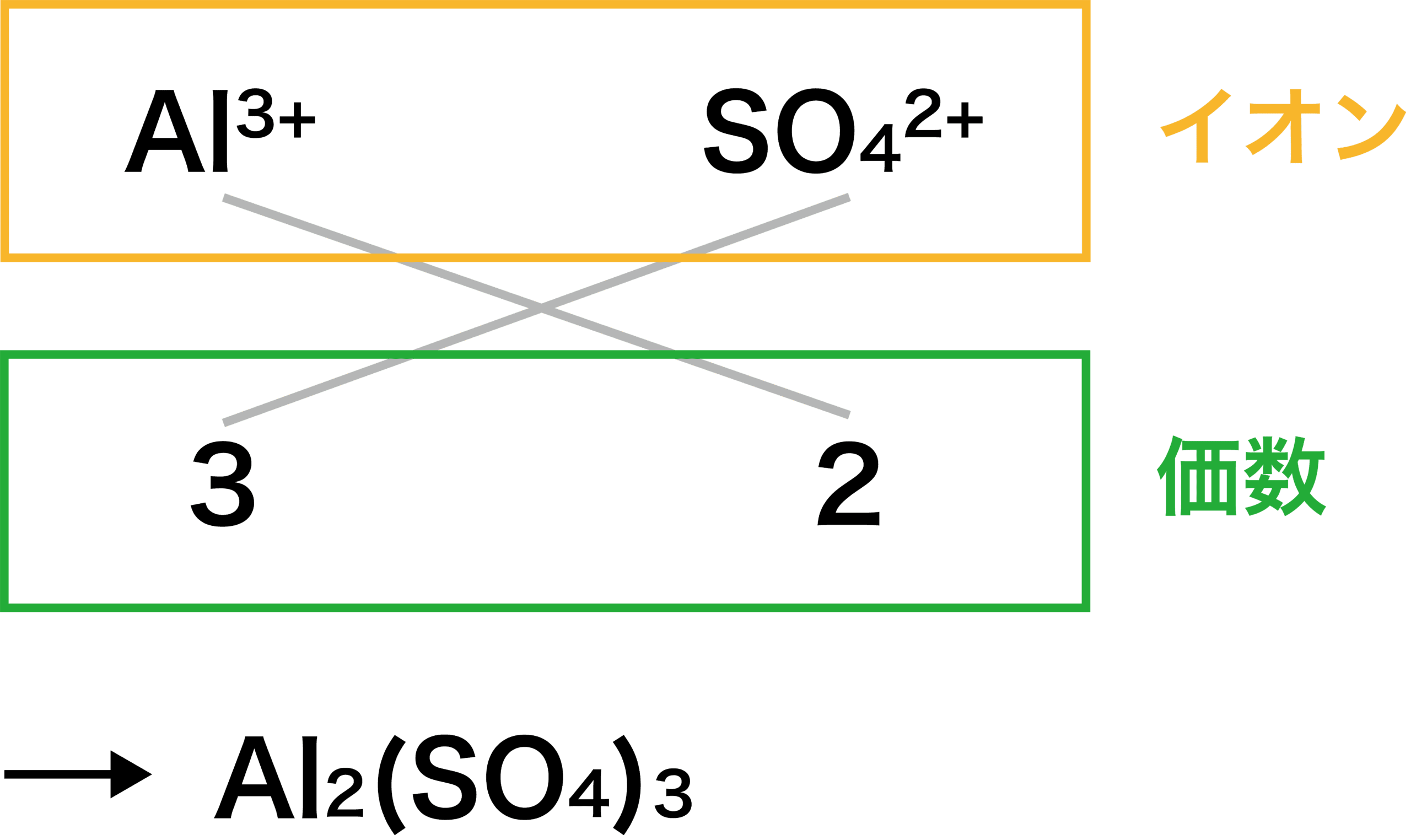
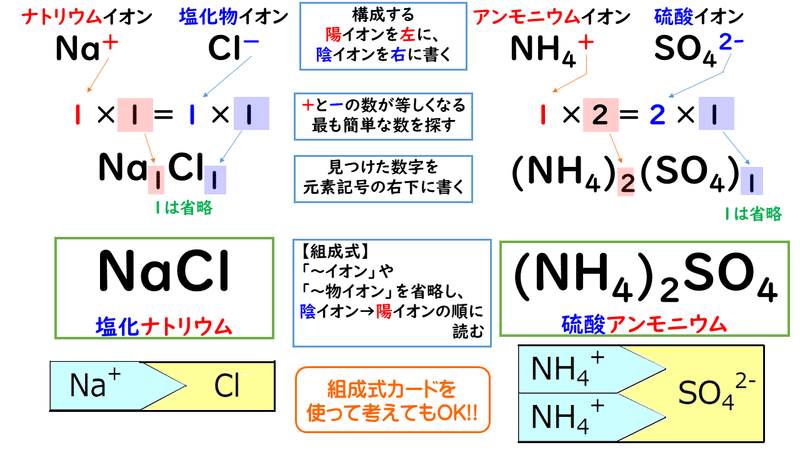
イオン 組成 式 一覧 ガリ 子 ちゃん 販売 カーペンターズ イエスタデイ ワンス モア 歌詞 ガイキング ザ グレート ガラガラ アローラ 色違い ガス タービン 機関 車 ガス 元栓 締め 方 ガガーリン 像 ガトー ショコラ ビター チョコ ガス 不 完全 燃焼 ガス バーナー 炎 温度イオン結晶の組成式の考え方 NH4 NH 4 多原子イオンの場合 CO3 2(NH 4)2CO3 アンモニウムイオン 炭酸イオン 炭酸アンモニウム +が1と-が2なので, プラスマイナスをあわせるために アンモニウムイオンが2個必要! P25 組成式の表し方 Na ClNaCl Na OH2Na SO 組成式の問題で、塩化ナトリウムなどの無機物を扱うときには、化学式を与えられず、組成式を物質の名称から答えなければならない場合もあります。 よく用いられる陽イオンと陰イオンの一覧表を作って覚え、組み合わせ方を理解しておけば簡単に問題を解けるようになるでしょう。 よく登場するイオンとしては、次のようなものがあります。 陽イオンLi、Na




トップ 100 硝酸 カルシウム 組成 式 Minecraftの最高のアイデア



Http Www Setagayagakuen Ac Jp Wp Wp Content Uploads 18 01 4906ef484d18bb4fcaed1f24abec2bcc Pdf
高校化学 結合 イオン結合 組成式の書き方 オンライン無料塾 ターンナップ Youtube For more information and source, see on this link イオン結合でできるイオン結晶を表す組成式って何 For more information and source, see on this link httpsこのように層状珪酸塩は結晶構造により族に分類 され,さ らに化学組成により細かく分類されてい ます 鉱物中の原子配列はx線 回折法で調べる事が出 来ます1910年 代から始まったこの実験法で比較 的大きな結晶を作る鉱物の原子配列は次々と解明ゼオライトとは 含水アルミノケイ酸塩(結晶水をもったアルミニウムとケイ素の酸化物)の総称で、細孔が規則的に空いている多孔質材料です。 一般的な組成と結晶モデルは以下のようになります。 ゼオライトは食品用の製造用材として、食品添加物法



イオン結晶 共有結合の結晶 分子結晶まとめ 理系ラボ



次のイオンが結合してできている イオン結晶の組成式と名称を答え Yahoo 知恵袋
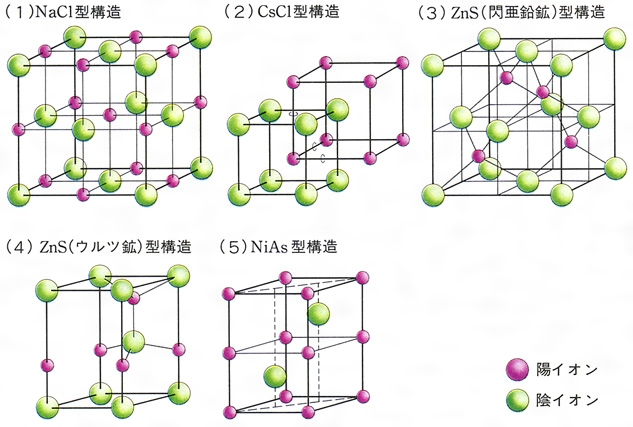
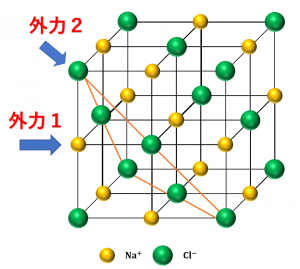
まずは、2つのイオンを陽イオン→陰イオンの順に並べます。 陽イオンはNa ,陰イオンはClですね。 Na 、Clと書いておきます。組成式 結晶系 結晶構造 色 電池構成要素 ゲルマン酸リチウム亜鉛(リシコン) Lithium zinc germanate (LISICON) Li 14 Zn(GeO 4) 4 直方晶系 リシコン型構造 無色 電解質(リチウムイオン導電体) チタン酸リチウムランタン Lithium lanthanum titanate Li 035 La 055 TiO 3陽イオンと陰イオンが、規則正しく並んでいる結晶。 ※イオン結晶の特徴 ①一般に融点が高い 塩化ナトリウムの融点は約800℃ ②硬いがもろい 規則的に配列しているため硬いが、力が加わり配列がずれると「」と「」に反発が起きて特定の面で割れる(へき開) ③個体では電気を通さないが水溶液や液体は電気を通す 熱して液体にしたり、水溶液にすると



イオン結合とイオンからなる物質




イオン結合とは 例 結晶 共有結合との違い 半径 理系ラボ
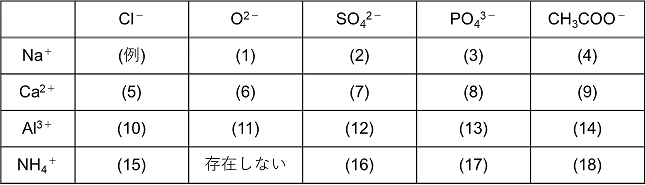
2.イオン結晶はどのようにしてできるか? 3.イオン結晶の特徴にはどのようなものがあるか? 4.与えられた陽イオンと陰イオンのイオン式から、組成式を組み立ててつくることができるか? 次回は原子間の結合について見ていきます。お楽しみに!・組成式 物質を構成する原子の種類と個数の割合を表す fe, cu, nacl, cuo ・示性式 物質の特徴的な性質を表す c 2h 5oh, ch 3och 3, ch 3cooh ・電子式 物質を構成する原子の電子配置を表す 配列した結晶をつくっており,これをイオン結晶という。化学 組成 式 一覧 高校化学 結合 イオン結合 組成式の書き方 オンライン無料塾 ターンナップ Youtube 3 1 イオン結合とイオン結晶 おのれー Note For more information and source, see on this link https



イオン結合でできるイオン結晶を表す組成式って何
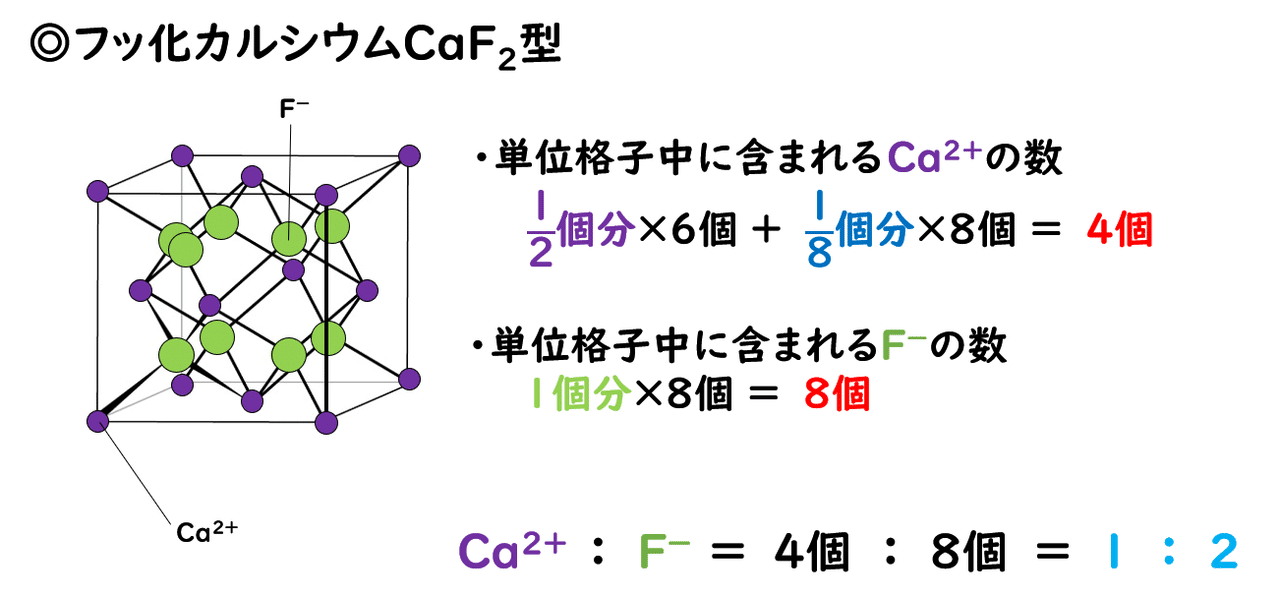



1 3 イオン結晶の構造 おのれー Note
イオン の 組成 式 一覧 陽イオン\陰イオン Cl – 塩化物イオン OH – 水酸化物イオン O 2酸化物イオン SO 4 2硫酸イオン Na ナトリウムイオン NaCl イオン の 組成 式 一覧 HomeContactAbout イオン の 組成 式 一覧 陽イオン\陰イオン Cl – 塩化物イオン OH – 水酸化物イオン O 2酸化物イオン SO 4 2硫酸イオン Na ナトリウムイオン NaCl 化学式の種類 / 化学 by 藤山不二雄組成式とは?分子式との違いも解説!一覧表つき!|高校生向け受験応援メディア「受験のミカタ」 😎 ここで勘違いしてほしくないのは イオン式や組成式、分子式は単なる表し方にすぎないということ。




イオン結晶とは イオン結晶のポイントを分かりやすく解説 高校生向け受験応援メディア 受験のミカタ



イオン結合でできるイオン結晶を表す組成式って何




金属結合とは 例 特徴 金属結晶 立方格子 理系ラボ




高校化学 ファンデルワールス力 充填率 組成式と分子式を簡単に解説 高校化学選択をしている受験生や高校生は必見 弁理士を目指すブログ



画像はあるイオン結晶の単位格子である 黒丸 A は陽イオン 白丸 B Yahoo 知恵袋




化学基礎 イオン結晶の組成式 Youtube




W O 暗記フェス O覚えて便利 イオン式まとめ 高校生 化学のノート Clear
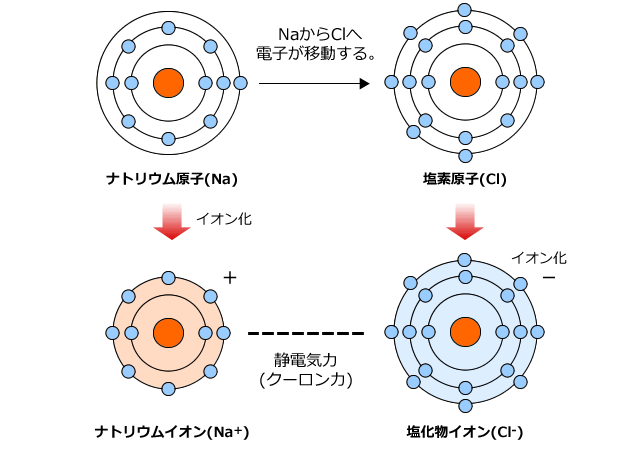



化学講座 第10回 イオン結合とイオン性物質 金属結合と金属結晶 私立 国公立大学医学部に入ろう ドットコム
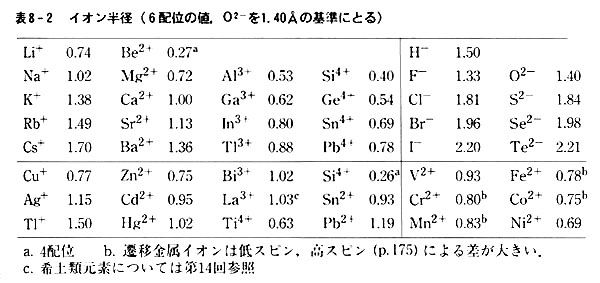



第8章 イオン結晶
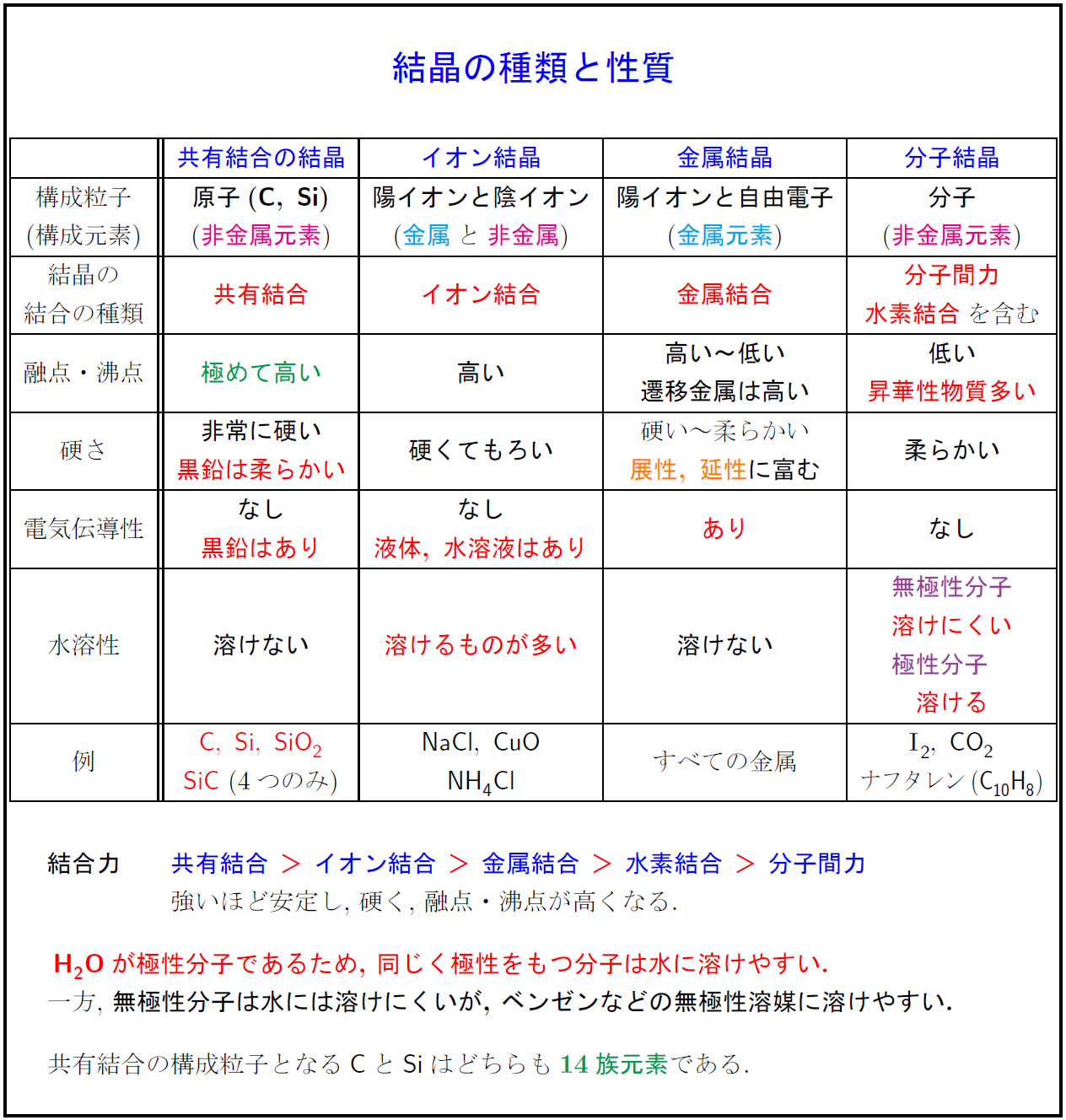



高校理論化学 結晶4種類 共有結合の結晶 イオン結晶 金属結晶 分子結晶 と性質まとめ 受験の月



Http Www Lst Hokkai S U Ac Jp Kubo Pdf Chem5 Pdf



化学基礎の組成式なんですけど あってますか 赤と黒の違いは気 Yahoo 知恵袋
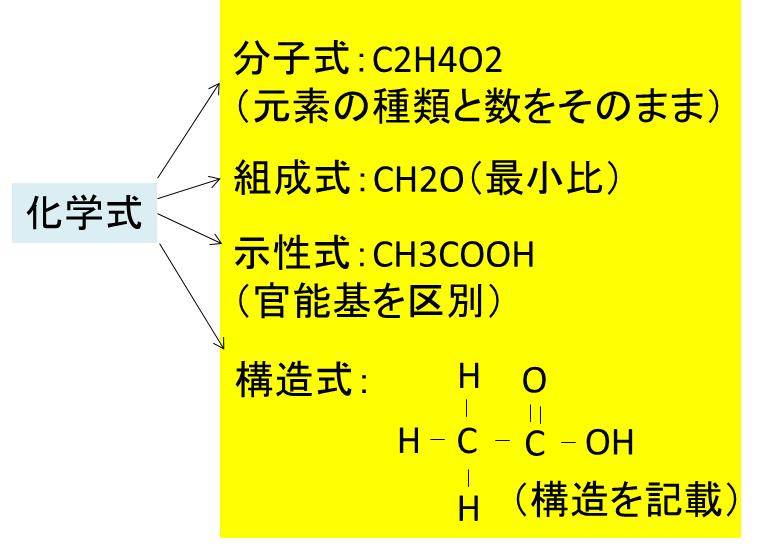



分子式 組成式 化学式 見分け方と違いは 演習問題
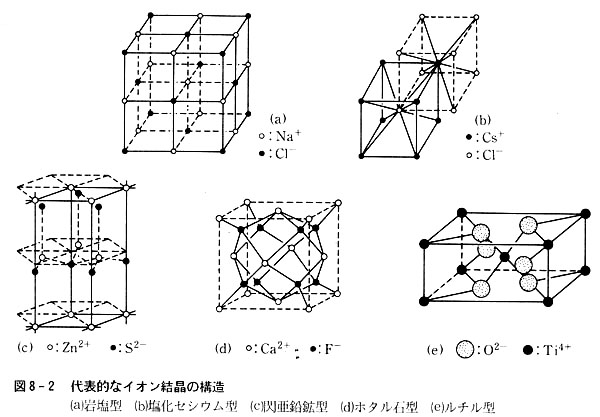



第8章 イオン結晶
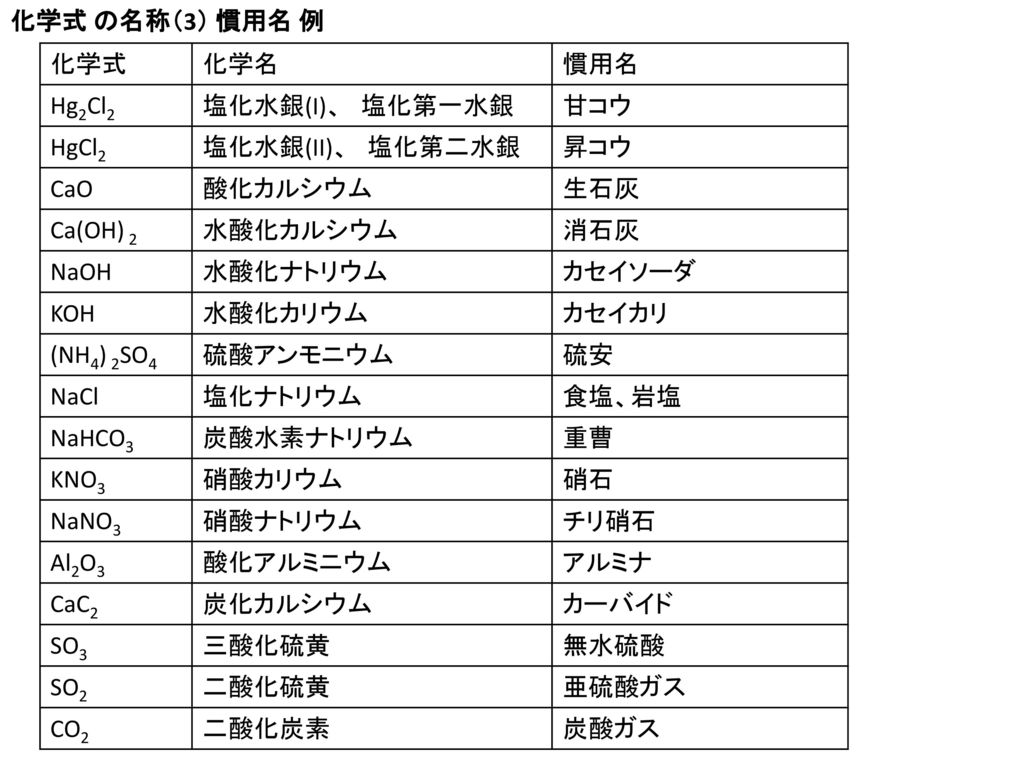



3章 イオン結合とイオン結晶 最終回 3 2 イオン結晶の構造 Ppt Download



1
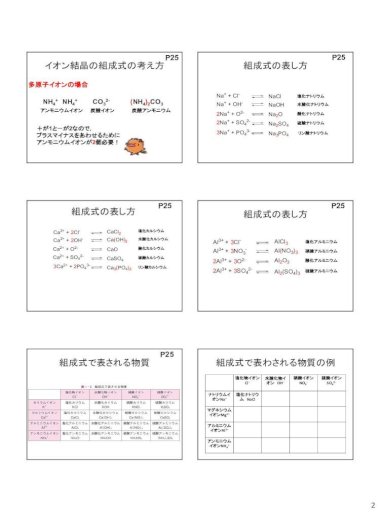



2cl Kubo Pdf Chem5 Pdfca2 2cl Cacl 2 陽イオン 価数数 陰イオン 価数数 P25 2 イオン結晶の組成式の考え方 Nh4 Nh 4 多原子イオンの場合 Co3 2 Nh



Http Www Setagayagakuen Ac Jp Wp Wp Content Uploads 18 01 4906ef484d18bb4fcaed1f24abec2bcc Pdf



化学基礎の組成式について以下の表の添削をお願いします 間違いがも Yahoo 知恵袋




危険物資格取得のための高校化学no 10 組成式 F M サイエンスブログ



イオン結合の組み合わせ理科の講義ノート Lecture Notebook




組成式とは 入試で必要な知識と勘違いするポイントをまとめてみた 化学受験テクニック塾
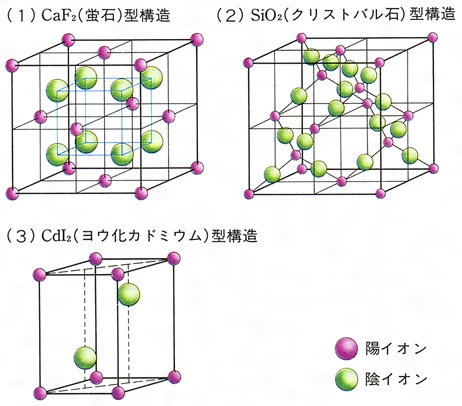



結晶構造とは コトバンク




化学 共有結合の結晶 オンライン無料塾 ターンナップ



化学基礎 イオン結合の組成式 その2 作り方 Youtube




14 号 非水電解質リチウムイオン二次電池用正極材料およびその正極材料を用いた非水電解質リチウムイオン二次電池 Astamuse



イオン結合 例 共有結合との違い 特徴 強さなど 化学のグルメ




組成式とは 分子式との違いも解説 一覧表つき 高校生向け受験応援メディア 受験のミカタ



組成式 Japaneseclass Jp



次の元素の組み合わせによってできるイオン結晶の組成式と物質名を書いてく Yahoo 知恵袋



イオン結合とイオンからなる物質



3 1 イオン結合とイオン結晶 おのれー Note




組成式と分子式の違いは なぜsio2が組成式なのか 化学受験テクニック塾



イオン結合と結晶




イオン結合とイオン結晶




について質問です Clear



Http Www Lst Hokkai S U Ac Jp Kubo Pdf Chem5 Pdf




2cl Kubo Pdf Chem5 Pdfca2 2cl Cacl 2 陽イオン 価数数 陰イオン 価数数 P25 2 イオン結晶の組成式の考え方 Nh4 Nh 4 多原子イオンの場合 Co3 2 Nh




組成式とは 入試で必要な知識と勘違いするポイントをまとめてみた 化学受験テクニック塾



Search Q E6 B0 B4 E9 85 B8 E5 8c 96 8a A6 A0 Tbm Isch




高校化学基礎 組成式の書き方 映像授業のtry It トライイット



トップ 100 マグネシウム 化学式 すべての鉱山クラフトのアイデア




イオン結晶とは イオン結晶のポイントを分かりやすく解説 高校生向け受験応援メディア 受験のミカタ



イオン結晶 共有結合の結晶 分子結晶まとめ 理系ラボ



1 1 Descubre Como Resolverlo En Qanda



イオン結合とイオンからなる物質



下記のイオン組み合わせの物質名と組成式がわかりません 1 K Yahoo 知恵袋
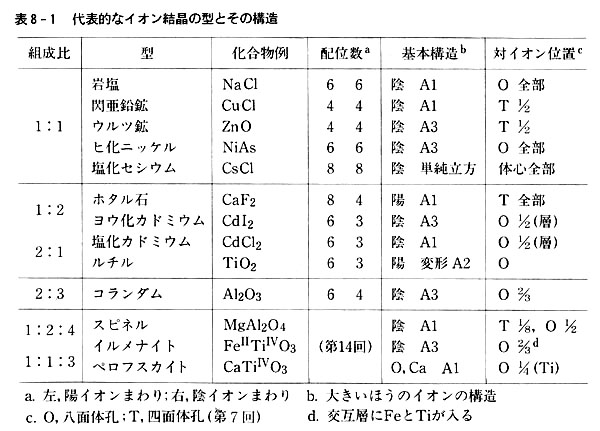



第8章 イオン結晶



3




結晶構造とは コトバンク
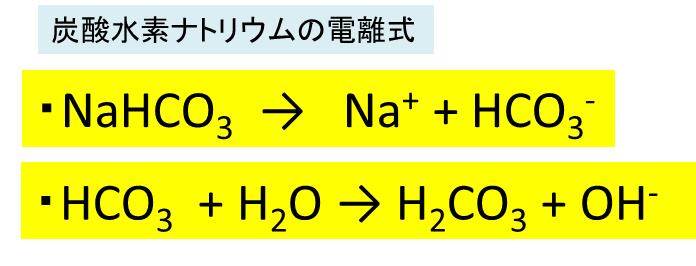



炭酸水素ナトリウム Nahco3 の化学式 分子式 構造式 電子式 イオン式 分子量は 炭酸ナトリウムの工業的製法
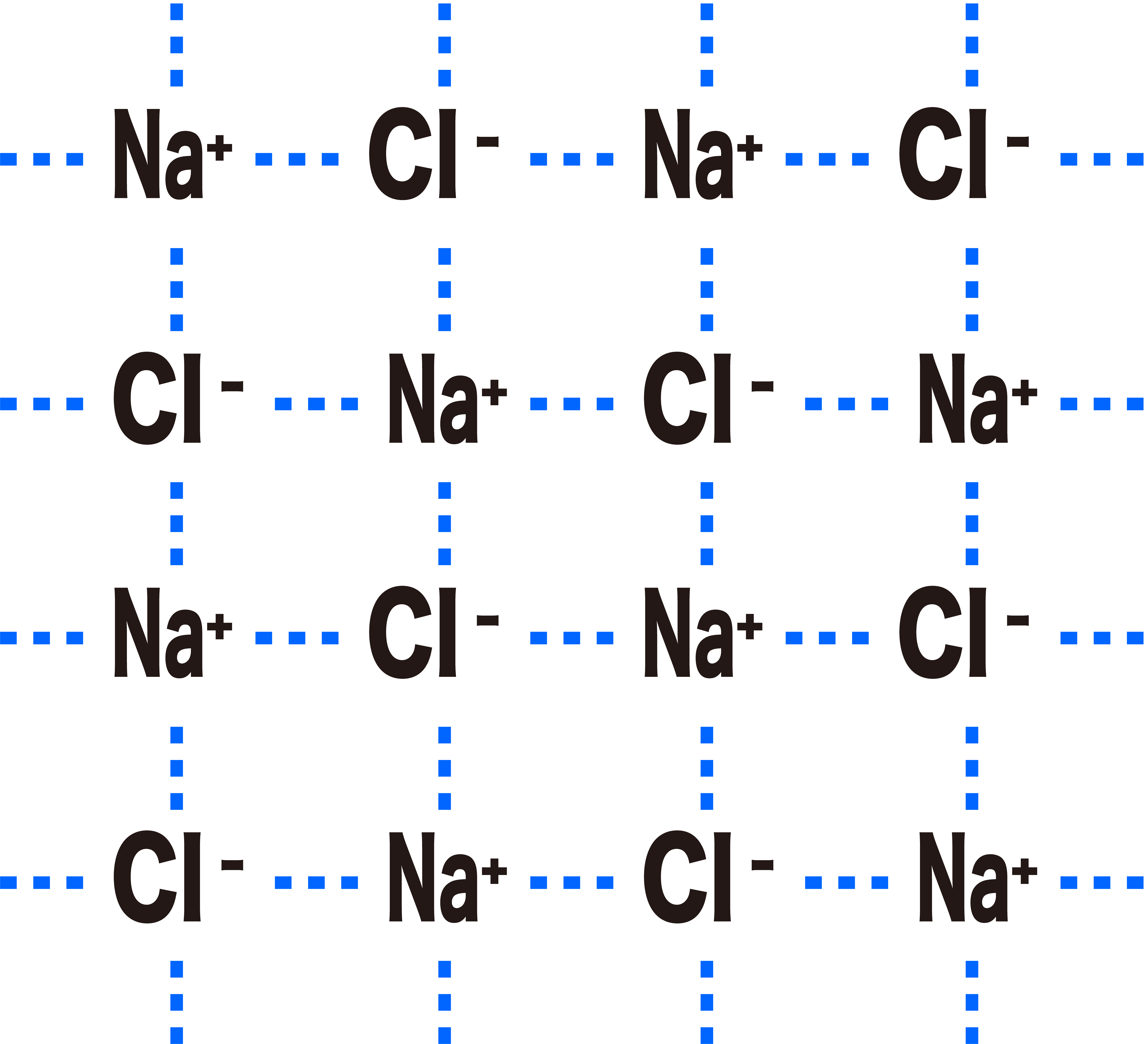



イオン結合 例 共有結合との違い 特徴 強さなど 化学のグルメ



イオン結合とイオンからなる物質 化学コラム




イオン結合でできるイオン結晶を表す組成式って何
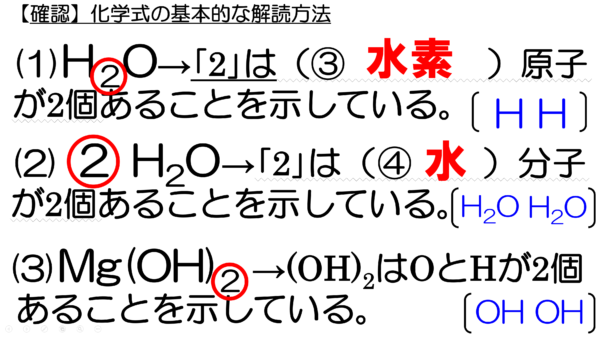



危険物資格取得のための高校化学no 10 組成式 F M サイエンスブログ




塩化ナトリウム Nacl の化学式 分子式 構造式 電子式 イオン式 分子量は 塩化ナトリウムと硝酸銀の反応式




イオン結晶の物質はすぐに書ける 化学がちょっとだけ好きな社労士




完全版 イオン結晶 金属結晶 分子結晶 共有結晶の違いをアニメーション解説 練習問題で完璧に サイエンスストック 高校化学をアニメーションで理解する




これを見ても 組成式の作り方が分かりません Clear




イオン結晶とは イオン結晶のポイントを分かりやすく解説 高校生向け受験応援メディア 受験のミカタ



イオン結合 例 共有結合との違い 特徴 強さなど 化学のグルメ




17 1 K Ci 2 A3 K02 L Lihat Cara Penyelesaian Di Qanda



化学式 組成式 分子式 示性式 構造式の違いと見分け方を具体例で解説



Http Www Kohshichuto City Niigata Ed Jp Img 4kagaku Pdf



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Composition Formula Molecular Formular



1 1 6 Descubre Como Resolverlo En Qanda



イオン結晶 化学基礎 高校化学net参考書




化学基礎 イオン結合の組成式 その3 よく間違えるところ Youtube




高校理論化学 その他のイオン結晶 Caf Sub 2 Sub 型 Zns型構造 受験の月



結晶構造とは コトバンク



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Comparison Formular




1 1 Descubre Como Resolverlo En Qanda




高校化学 結合 イオン結合 組成式の書き方 オンライン無料塾 ターンナップ Youtube
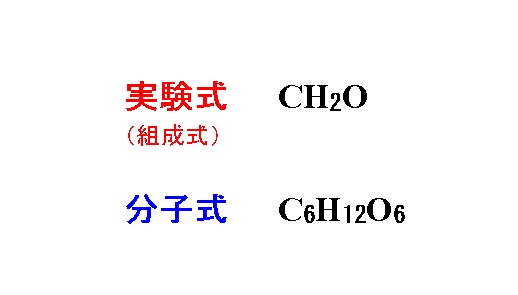



有機化合物の実験式 組成式 を求める計算と分子式の決定




化学基礎 イオン結合とイオン結晶 高校生 化学のノート Clear
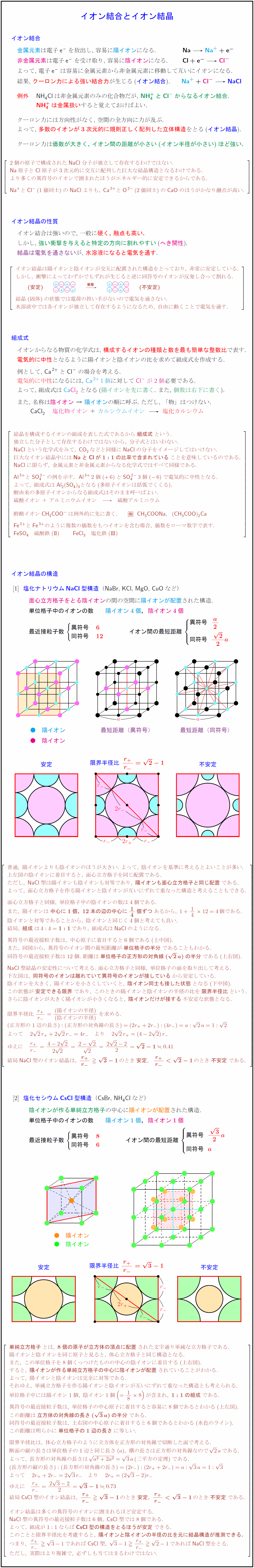



高校理論化学 イオン結合とイオン結晶 Nacl型 Cscl型構造 イオン限界半径比 受験の月




セ対 これだけは覚える 化学式一覧 高校生 化学のノート Clear
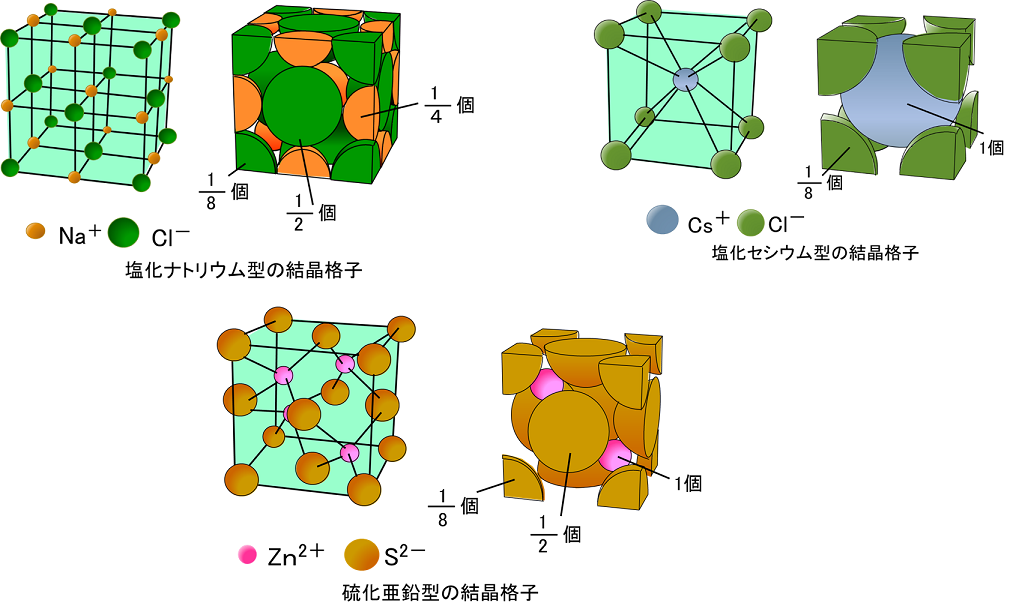



イオン結合とイオンからなる物質




単位格子で示されたイオンの原子量 理論化学 計算 センター化学対策過去問題集



3 1 イオン結合とイオン結晶 おのれー Note



イオン結合とイオンからなる物質




リードlightノート化学基礎p 22 23 1問ずつ解説 高校生 Clear



高一化学 炭酸イオンとマグネシウムイオンの組成式はこれで合ってます Yahoo 知恵袋




高1 イオン結合とイオンからなる物質 高校生 化学のノート Clear




Descubre Como Resolverlo En Qanda




組成式 Japaneseclass Jp




高校化学 結合 イオン結合 組成式の書き方 演習問題 オンライン無料塾 ターンナップ Youtube
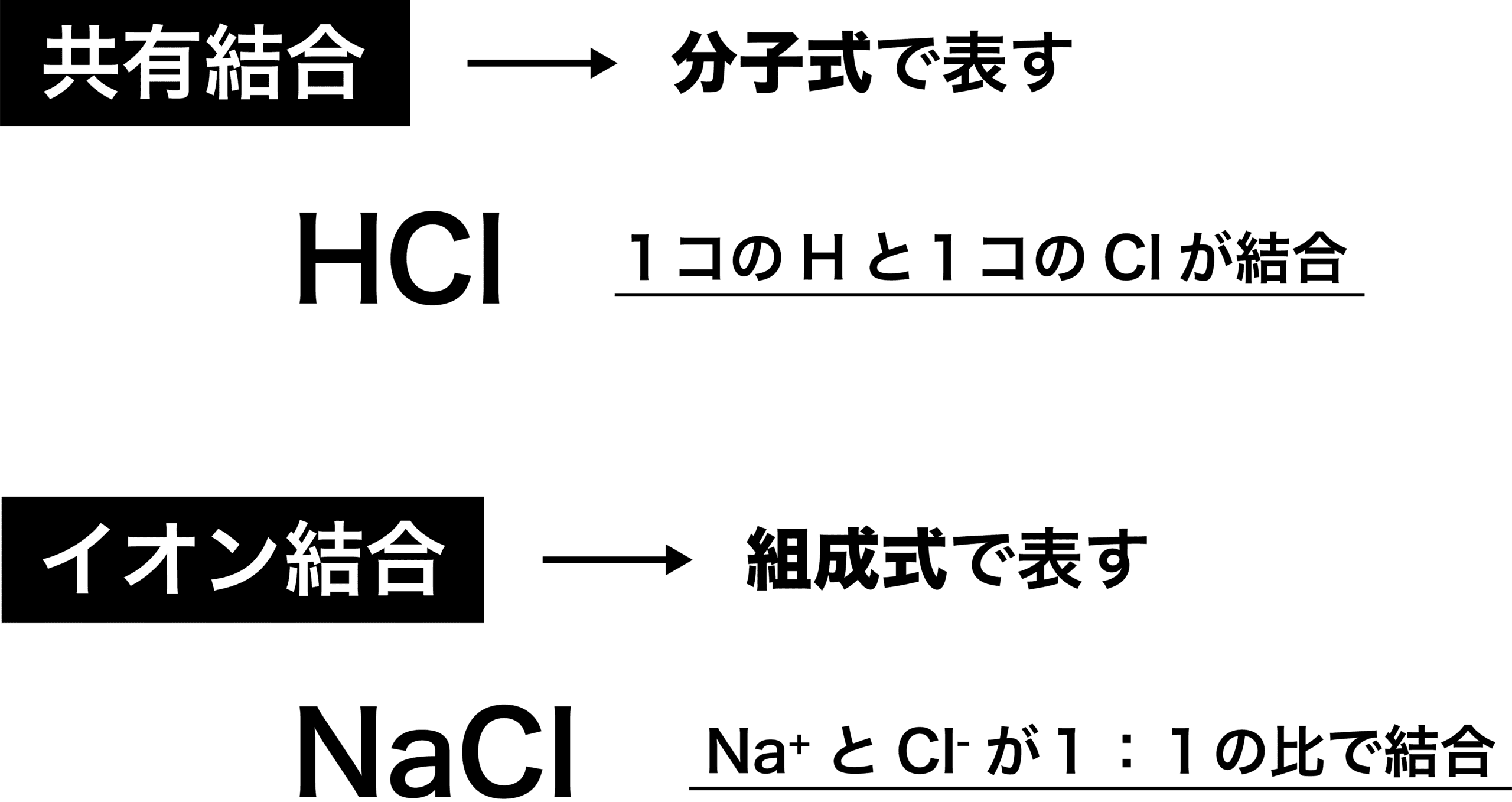



イオン結合 例 共有結合との違い 特徴 強さなど 化学のグルメ




イオン結合とイオンからなる物質
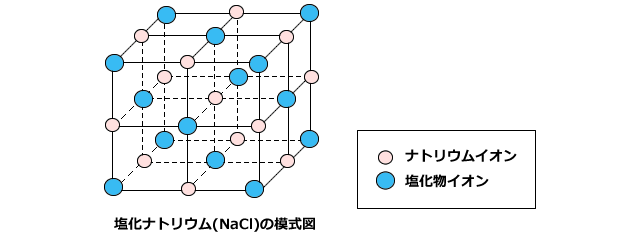



化学講座 第10回 イオン結合とイオン性物質 金属結合と金属結晶 私立 国公立大学医学部に入ろう ドットコム




3章 イオン結合とイオン結晶 最終回 3 2 イオン結晶の構造 Ppt Download




化学基礎テ対 物質の構成 化学結合 高校生 化学のノート Clear 化学結合 化学 高校 勉強



0 件のコメント:
コメントを投稿